إن الأكسجين لهو أحد العوامل الرئيسية التي تحتاجها خلايانا للقيام بوظائفها، ومع ذلك فلطالما كانت العملية التي تتكيف بها الخلايا مع تغير معدل توفّر الأكسجين بالجسم غامضةً لفترة طويلة، لكن هذا الغموض يحمل بين ثناياهُ الكثير من الطُّرق التي يمكنها معالجة الكثير من الأمراض مثل "الأنيميا" فقر الدم والجلطات والسرطان والسكتات الدماغيّة والكثير من الأمراض الأخرى.
مُعضلة أزلية
ثلاثةٌ من العلماء تحدّوا أنفسهم لسنواتٍ طويلة حتى استطاعوا معرفة هذا السّر الغامض الذي نالوا به نوبل 2019 في الطب؛ ألا وهم (جريج سمينزا من جامعة هوبكنز - راتكليف من جامعة أوكسفورد - ويليام كايلين من جامعة هارفارد) إنهم ثلاثي أضواء المسرح اليوم عن اكتشافاتهم للطريقة التي تستشعر بها الخلايا وجود الأكسجين وتكيّفها مع تغير مستواه بالدم. واحدة من أهم الآليات في الحياة وحجر الأساس لفهمنا كيفية تأثير مستويات الأكسجين على عملية الأيض الخلوية والوظيفة الفسيولوجية. حيث مهد اكتشافهم الطريق لاستراتيجيات جديدة واعدة لمكافحة العديد من الأمراض.
ثلاثي أضواء المسرح

قام جريج سمينزا - الأستاذ بجامعة جونز هوبكنز منذ عام 1999، ومدير برنامج أبحاث الأوعية الدموية في معهد جونز هوبكنز لهندسة الخلايا منذ عام 2003 - بعمل تجارب على بعض الفئران المعدلة وراثيًا وتتبع تغيّر مستوى الأكسجين، حتى وجد أن الاستجابة الأساسية لنقصه تتمثل في ارتفاع مستويات أحد الهرمونات والتي تُسمى EPO الإريثروبويتين Erythropoietin، ومع زيادة التدقيق وجد أن جزءًا محددًا من الحمض النووي يقع بجانب جين الـ EPO هو الذي يتجاوب مع نقص الأكسجين.
قام «بيتر راتكليف» - مدير الأبحاث السريرية في معهد فرانسيس كريك في لندن، وعضو في معهد لودفيج لأبحاث السرطان، ومدير معهد "تارجيت ديسكفري" في مدينة أكسفورد. - أيضًا بدراسة التنظيم المعتمد على الأكسجين لجين EPO، وكان نتاج كلا الدراستين أن آلية استشعار الأكسجين كانت موجودة في جميع الأنسجة تقريبًا، وليس فقط في خلايا الكلى التي يتم فيها إنتاج EPO بشكل طبيعي.
مركب "HIF-1 Alpha"
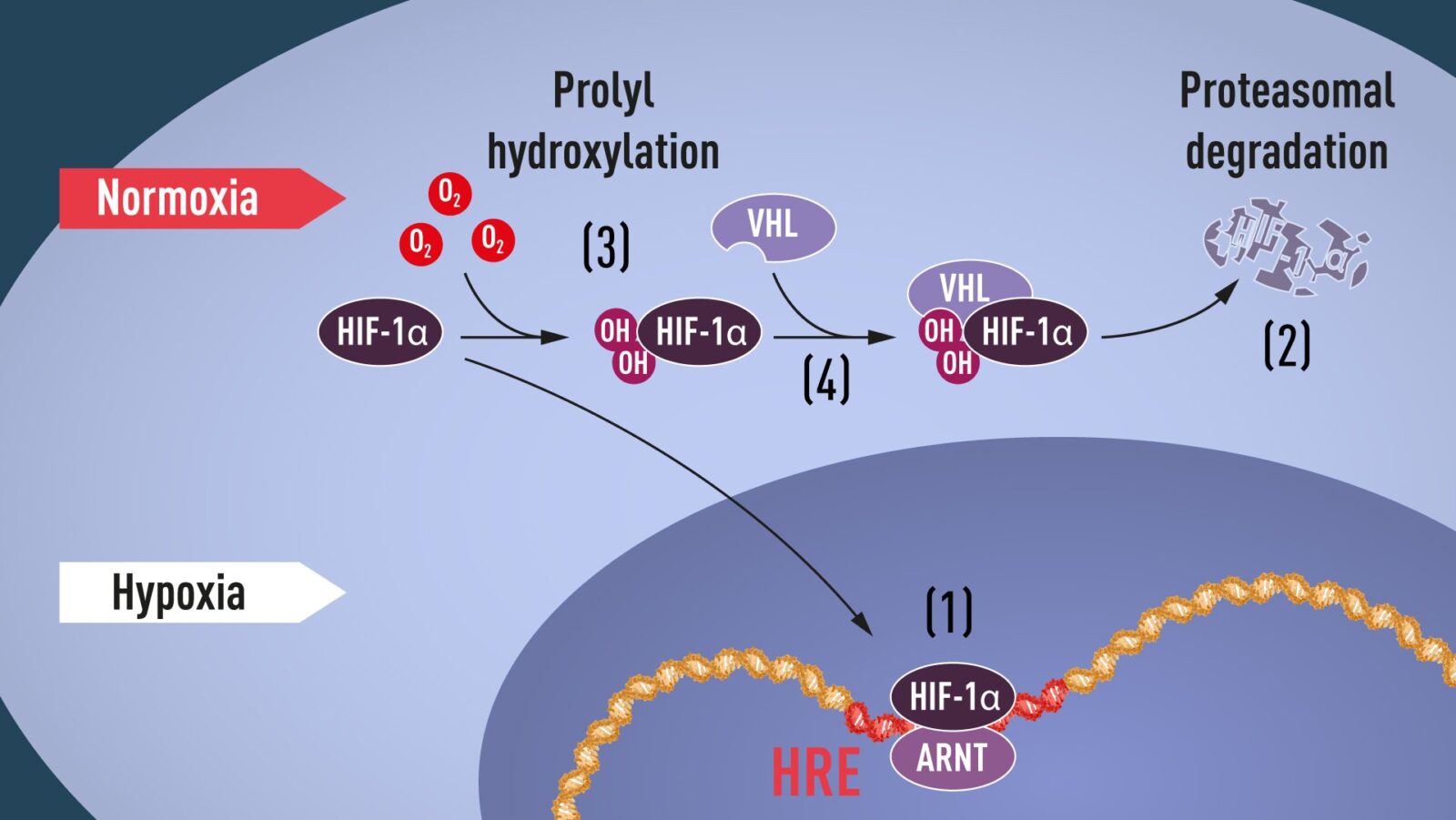
باستكمال تجاربه في خلايا الكبد المزروعة، اكتشف العالم سيمنزا مركب بروتيني هام يرتبط بجزيء الحمض النووي ويعمل اعتمادًا على الأكسجين، وسُمي هذا المركب باسم "HIF-1 Alpha" أو «العوامل المحفّزة لنقص الأكسجين» وأهمية تلك الدراسات أنها تُبين أن الآلية كانت عامة ووظيفية في العديد من أنواع الخلايا المختلفة.
عندما يحدث تغيّر في معدلات الأكسجين في الجسم، تستطيع الخلايا الاستجابة لهذه التغيّرات عبر استخدام الآلية الجزيئية التي تساعد على تنظيم نشاط الجينات؛ فعندما تنخفض نسبة الأكسجين تحافظ الخلية على بروتين HIF-1 Alpha وتمنع تحلُّله، مما يزيد من تراكمه في النواة، ليرتبط مع تسلسل حمض نووي "DNA" مُحدد في الجينات التي تُنظم عملية نقص الأكسجين. أما في الظروف العادية التي يكون فيها مستوى الأكسجين طبيعيًّا، فإن الـHIF-1 Alpha يتحلل سريعًا بواسطة البروتيزوم، - وهو مركَّب بروتيني يتولى عملية التفكيك- ويتولى الأكسجين تنظيم عملية التحلُّل هذه عبر إضافة مجموعات هيدروكسيل OH إلى الـHIF-1 Alpha.
في نفس الوقت الذي كان سيمينزا وراتكليف يكشفان عملية تنظيم جين الـ EPO، عكف باحث السرطان ويليام كيلين على كشف أسرار حالة وراثية غريبة، تُعرف باسم (VHL)”فون هيبل لينداو” Von Hippel Lindau وهي حالة مرضية تؤدي لزيادة كبيرة في خطر الإصابة ببعض أنواع السرطان في العائلات التي تحمل طفرات الـ VHL الموروثة.
اكتشف كايلين أن جين VHL هذا ينتج بروتينًا يمنع حدوث السرطان، ووجد أيضًا أن الخلايا السرطانية التي تفتقر إلى جين الـ VHL الوظيفي السليم، تعبر -بشكل غير طبيعي- عن مستويات عالية من الجينات المنظمة لنقص الأكسجة؛ ولكن عندما أعيد إدخال جين الـ VHL في الخلايا السرطانية، استعادت المستويات الطبيعية. كان هذا دليلًا مهمًا يوضح أن جين الـ VHL متورطًا بطريقة ما في التحكم في الاستجابة لنقص الأكسجة.
وأخيرًا،
فإن الفشل الكلوي هو مشكلة كبيرة أيضًا بسبب نقص هرمون يمكن زيادته إذا رفعنا من مستوي "HIF-1 Alpha"، أما مصابي السرطان فلديهم زيادة في نشاط "HIF-1 Alpha" مما يساعد الخلايا السرطانية على النمو والتشعب؛ فربما نستطيع ابتكار دواء ما يساعد علي تثبيط "HIF-1 Alpha" وهكذا في نطاق واسع جدًا من الأمراض مثل الأنيميا وأمراض القلب والجلطات والسكتات الدماغية.